QPCTL
Une petite molécule inhibitrice de QPCTL comme traitement potentiel des tumeurs avec un engagement élevé de l'axe α de la protéine régulatrice du signal CD47
(« SIRPα ») (Phase I)
(« SIRPα ») (Phase I)
Analyses terminées
Co-development with Fosun
- In vivo anti-tumor efficacy studiesCombo study with Rituximab, anti-PD-1, or paclitaxel, Azacytidine
-
 In vivo efficacy studies
In vivo efficacy studies
with single agent -
 In vivo PK-PD
In vivo PK-PD -
 In vivo PK studies
In vivo PK studies - In vivo acute efficacy studies
-
 In vitro ADMET studies
In vitro ADMET studies -
 Developability/CMC
Developability/CMC -
 In vitro cell-based
In vitro cell-based -
 Toxicology studies
Toxicology studies - Enzymatic
Justification de la cible
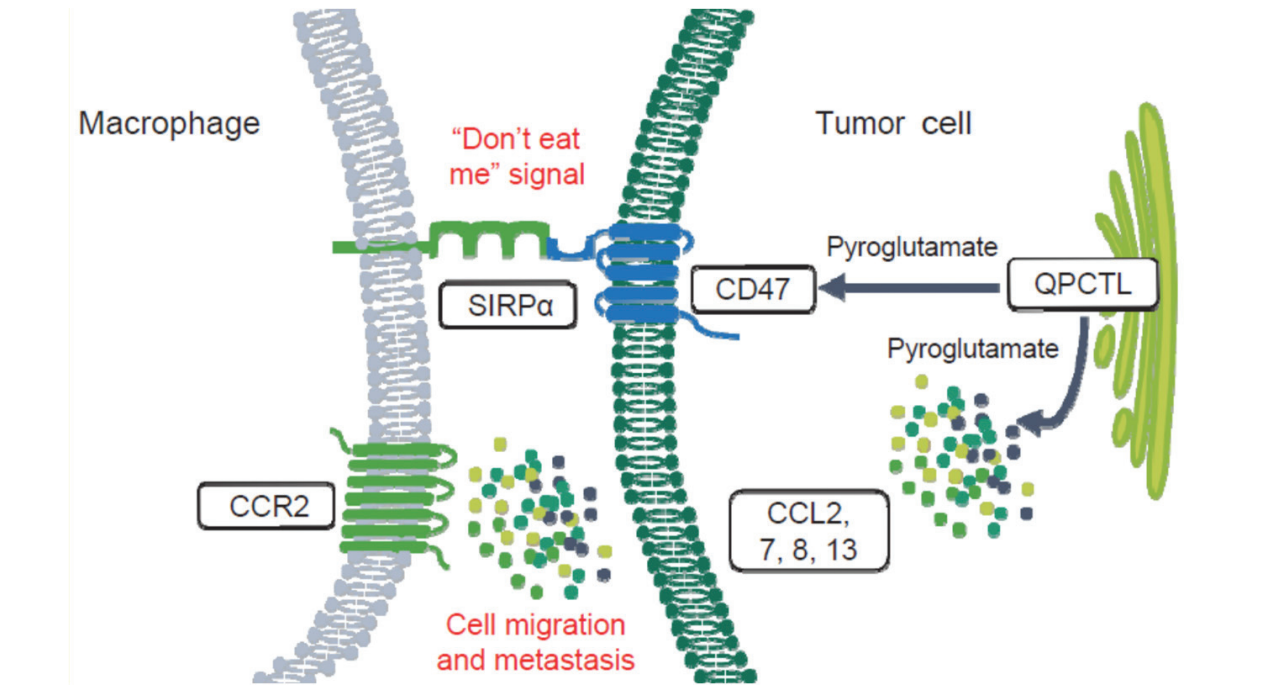
QPCTL, qui est situé sur l’organite cellulaire appelé appareil de Golgi, a été identifié comme un régulateur crucial de l’axe CD47-SIRPα, communément appelé axe « ne me mange pas ».
Il a été démontré que l'inhibition de QPCTL avec des outils pharmacologiques ou des méthodes d'inactivation issues de la bio-ingénierie provoque une réduction ou une perte de la liaison entre CD47 et SIRPα, ainsi qu'une phagocytose cellulaire dépendante des anticorps et une cytotoxicité induite par les neutrophiles. Compte tenu de l'absence d'appareil de Golgi où QPCTL est localisé dans les érythrocytes matures, les inhibiteurs de QPCTL peuvent induire une toxicité hématologique plus faible que la plupart des agents bloquant le CD47 actuellement en développement clinique.
De plus, la régulation négative de la transduction de signalisation CCL2/CCR2 en inhibant QPCTL pourrait être utilisée pour reprogrammer le microenvironnement immunitaire de la tumeur en modulant les cellules myéloïdes suppressives vers un profil enrichi en macrophages phagocytaires, transformant ensuite des tumeurs moins enflammées par les lymphocytes T en une tumeur fortement infiltrante par les lymphocytes T, et favorisent en outre l’immunité anti-tumorale dirigée par des activateurs de lymphocytes T comme les anticorps anti-PD-1/L1.
Il a été démontré que l'inhibition de QPCTL avec des outils pharmacologiques ou des méthodes d'inactivation issues de la bio-ingénierie provoque une réduction ou une perte de la liaison entre CD47 et SIRPα, ainsi qu'une phagocytose cellulaire dépendante des anticorps et une cytotoxicité induite par les neutrophiles. Compte tenu de l'absence d'appareil de Golgi où QPCTL est localisé dans les érythrocytes matures, les inhibiteurs de QPCTL peuvent induire une toxicité hématologique plus faible que la plupart des agents bloquant le CD47 actuellement en développement clinique.
De plus, la régulation négative de la transduction de signalisation CCL2/CCR2 en inhibant QPCTL pourrait être utilisée pour reprogrammer le microenvironnement immunitaire de la tumeur en modulant les cellules myéloïdes suppressives vers un profil enrichi en macrophages phagocytaires, transformant ensuite des tumeurs moins enflammées par les lymphocytes T en une tumeur fortement infiltrante par les lymphocytes T, et favorisent en outre l’immunité anti-tumorale dirigée par des activateurs de lymphocytes T comme les anticorps anti-PD-1/L1.
Résumé des inhibiteurs de QPCTL d’Insilico Medicine – Phase I
Nouvelle structure générée par l'IA
- Structure distinctement différente générée par la plateforme de génération de petites molécules d'IA d'Insilico Medicine, Chemistry42
Immunothérapie efficace contre le cancer
- Puissante activité inhibitrice de la liaison de SIRP-α aux cellules cancéreuses exprimant CD47
- Nouvelle classe d'E/S utilisant l'immunité innée et renforçant davantage l'immunité adaptative grâce à la reprogrammation du paysage myéloïde tumoral vers un profil anti-tumorigène
- Larges indications potentielles incluant à la fois le LNH/LMA et les tumeurs solides
Capacité médicamenteuse prometteuse en tant qu’agent oral
- Bons profils ADME in vitro
- Profils pharmacocinétiques prometteurs pour différentes espèces animales précliniques
Marge de sécurité favorable
- MOS prometteur chez le rat et le chien basé sur des études BPL sans toxicité hors cible évidente
- Nettoyer sur la pharmacologie de sécurité
Indication
La détection et l'élimination des cellules cancéreuses via la phagocytose induite par des points de contrôle immunitaires innés jouent un rôle important dans l'évasion immunitaire médiée par la tumeur. L'axe CD47-SIRPα, dont la signalisation est soutenue par QPCTL, est le point de contrôle immunitaire inné le mieux décrit qui permet aux cellules cancéreuses exprimant CD47 d'échapper à la phagocytose médiée par les cellules immunitaires innées. Les agents qui bloquent l'interaction CD47-SIRPα sont actuellement évalués dans plusieurs essais en cours, la plupart en association avec des agents pro-phagocytose, par ex. anticorps thérapeutiques, chimiothérapie chez les patients atteints de leucémie, de lymphome et de tumeurs solides avancées (carcinome épidermoïde de la tête et du cou, cancer gastrique, cancer du sein, cancer colorectal, etc.). L'inhibiteur QPCTL pourrait être développé pour les patients présentant ces indications, en particulier lorsqu'ils sont résistants aux thérapies standard, par ex. azacytidine, rituximab, paclitaxel, trastuzumab, cetuximab, etc.
Statut du projet – Phase I
Actuellement co-développé en partenariat avec Fosun, un inhibiteur de petite molécule de QPCTL, un régulateur de l'axe CD47-SIRPα, disponible par voie orale, comme immunothérapie anticancéreuse. Les résultats préliminaires ont démontré une puissante activité inhibitrice enzymatique, une forte efficacité et des effets synergiques avec d’autres thérapies. Nous avons déposé une demande d'IND auprès de la NMPA en Chine en avril 2023 et prévoyons de lancer l'essai clinique de phase I au cours du second semestre 2023.
Découvert en tirant parti de notre plateforme Pharma.AI. Nous avons utilisé les capacités d'identification de cibles et de business intelligence de PandaOmics pour identifier de nouvelles cibles en oncologie, et QPCTL a été répertorié parmi les nouvelles cibles médicamenteuses prometteuses ayant des implications dans l'axe CD47-SIRPα. Nous avons ensuite utilisé la chimie générative pour générer ISM8207 contre QPCTL pour le traitement des tumeurs avec un engagement élevé de l'axe CD47-SIRPα.
Découvert en tirant parti de notre plateforme Pharma.AI. Nous avons utilisé les capacités d'identification de cibles et de business intelligence de PandaOmics pour identifier de nouvelles cibles en oncologie, et QPCTL a été répertorié parmi les nouvelles cibles médicamenteuses prometteuses ayant des implications dans l'axe CD47-SIRPα. Nous avons ensuite utilisé la chimie générative pour générer ISM8207 contre QPCTL pour le traitement des tumeurs avec un engagement élevé de l'axe CD47-SIRPα.
