PHD1/2 — MII
Une petite molécule inhibitrice de PHD1/2 pour le traitement des MII (Phase I)
Analyses terminées
Owned and Available for Licensing
- In vivo efficacy studiesCombo study with Mesalamine,
Anti-TNFα antibody and CsA - In vivo efficacy studies
with single agent -
 In vivo PK studies
In vivo PK studies -
 In vitro ADME studies
In vitro ADME studies -
 Developability/CMC
Developability/CMC -
 In vitro cell-based
In vitro cell-based -
 Toxicology studies
Toxicology studies - Enzymatic
Justification de la cible
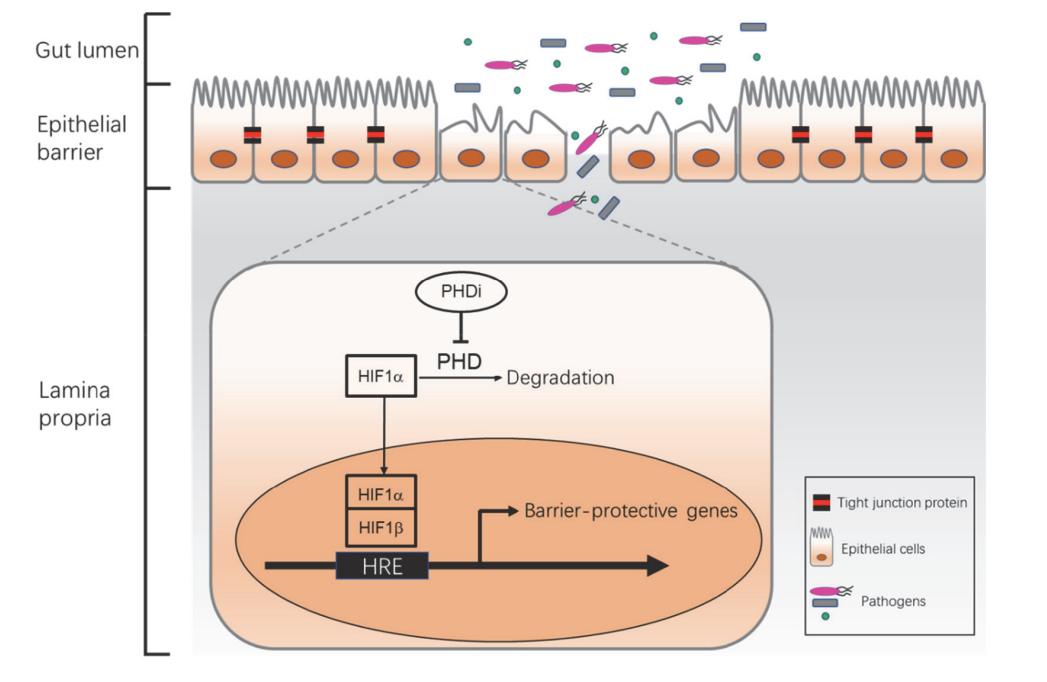
Les HIF ont plus récemment été reconnus comme un régulateur protecteur des MII en se liant à l'HRE et en pilotant l'expression de gènes protecteurs de barrière. Les PHD sont responsables de l’hydroxylation de HIFα, qui initie la voie qui aboutit finalement à la dégradation de HIFα par le protéasome.
L'inhibition des PHD, en particulier PHD1 et PHD2, réduit la dégradation de HIFα et un niveau plus élevé de HIF conduit à l'expression de gènes protecteurs de barrière pour la guérison de la barrière épithéliale et à une diminution de l'expression des cytokines proinflammatoires. Cependant, étant donné que les facteurs de transcription HIF sont impliqués dans la régulation de processus biologiques étendus, une exposition systématique aux inhibiteurs de la PHD peut augmenter le risque de tumeur maligne, de rétinopathie, de thrombose, d'hyperkaliémie et d'hypertension artérielle. Par conséquent, l’administration orale d’inhibiteurs doubles PHD1 et PHD2 restreints à l’intestin peut constituer une stratégie clinique innovante pour les patients atteints de MII.
L'inhibition des PHD, en particulier PHD1 et PHD2, réduit la dégradation de HIFα et un niveau plus élevé de HIF conduit à l'expression de gènes protecteurs de barrière pour la guérison de la barrière épithéliale et à une diminution de l'expression des cytokines proinflammatoires. Cependant, étant donné que les facteurs de transcription HIF sont impliqués dans la régulation de processus biologiques étendus, une exposition systématique aux inhibiteurs de la PHD peut augmenter le risque de tumeur maligne, de rétinopathie, de thrombose, d'hyperkaliémie et d'hypertension artérielle. Par conséquent, l’administration orale d’inhibiteurs doubles PHD1 et PHD2 restreints à l’intestin peut constituer une stratégie clinique innovante pour les patients atteints de MII.
Insilico Medicine PHD — Résumé des inhibiteurs de la MII – Phase I
Nouvelle structure générée par l'IA
- Structure distinctement différente générée par la plateforme de génération de petites molécules d'IA d'Insilico Medicine, Chemistry42
Efficace dans les thérapies mono et combo
- Puissante inhibition enzymatique PHD1/2
- Puissante induction de HIF-1α
- Monothérapie efficace dans les modèles de colite TNBS et DSS
- Thérapie combinée efficace avec des médicaments anti-inflammatoires dans les modèles de colite TNBS et DSS
Capacité médicamenteuse prometteuse en tant qu’agent oral
- Bons profils ADME in vitro
- Profils pharmacocinétiques restreints à l’intestin prometteurs chez différentes espèces animales précliniques
Marge de sécurité favorable
- MOS prometteurs dans les études sur le rat et le chien
- Profils de sécurité in vitro favorables
Indication
La maladie inflammatoire de l'intestin (MII) est caractérisée par une inflammation du côlon et de l'intestin grêle, conduisant à une colite ulcéreuse et à la maladie de Crohn. La colite ulcéreuse touche principalement le côlon et le rectum, tandis que la maladie de Crohn touche l'ensemble du tractus gastro-intestinal. Ces maladies se caractérisent par une inflammation chronique et des lésions de la muqueuse ainsi que par une perte de la fonction de barrière épithéliale intestinale.
Statut du projet – Phase I
Un inhibiteur oral de petite molécule de PHD1/2, restreint à l'intestin, pour le traitement des MII, terme générique désignant les troubles impliquant une inflammation chronique du tube digestif, tels que la colite ulcéreuse et la maladie de Crohn. Les études précliniques montrent qu'ISM5411 est bien toléré et démontre son efficacité dans plusieurs modèles de colites murines induites par différents produits chimiques. Nous avons lancé des études permettant l'IND et prévoyons de déposer nos demandes d'IND en Chine et aux États-Unis au cours du second semestre 2023.
Découvert en tirant parti de notre plateforme Pharma.AI.
Découvert en tirant parti de notre plateforme Pharma.AI.
PHD1/2 — CKD
Une petite molécule inhibitrice de PHD1/2 comme traitement potentiel de l'anémie de l'IRC (Phase I)
Analyses terminées
Owned and Available for Licensing
-
 In vivo efficacy studies
In vivo efficacy studies
with single agent -
 In vivo PK-PD
In vivo PK-PD -
 In vivo PK studies
In vivo PK studies -
 In vitro ADME studies
In vitro ADME studies -
 Developability/CMC
Developability/CMC -
 In vitro cell-based
In vitro cell-based -
 Toxicology studies
Toxicology studies - Enzymatic
Justification de la cible
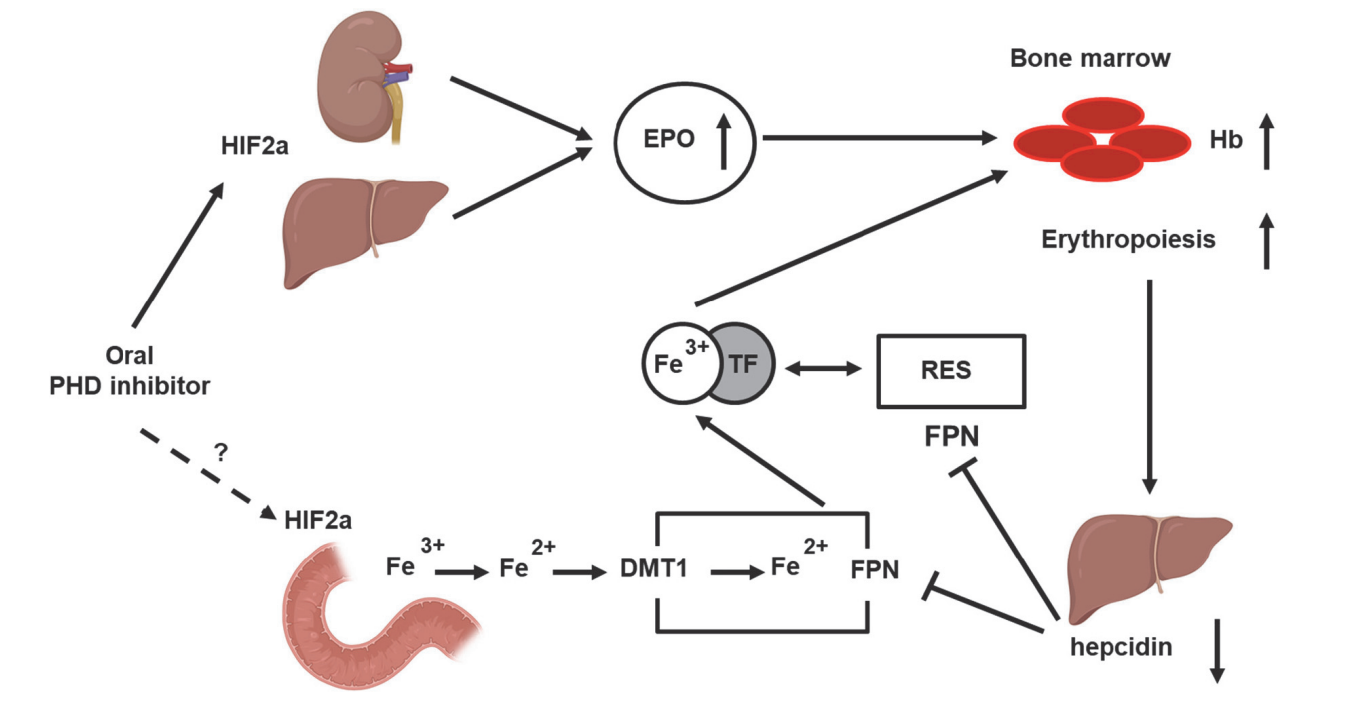
L'anémie de l'IRC est une forme d'anémie normocytaire normochrome et hypoproliférative. La dernière étape moléculaire qui contrôle la stabilisation des HIF converge vers les prolyl hydroxylases (« PHD »). Les PHD hydroxylent HIFα, une sous-unité de HIF, conduisant à la dégradation de HIFα par le protéasome. Parmi trois sous-types de PHD, à savoir PHD1, PHD2 et PHD3, PHD2 démontre une expression plus abondante dans tous les types de tissus par rapport aux autres sous-types et l'inhibition de PHD2 a été indiquée comme traitement prometteur pour les maladies liées à HIFα.
L'inhibition de PHD1/2 pourrait réguler positivement l'expression de plusieurs gènes du métabolisme du fer, tels que le transporteur de métaux divalents 1 (« DMT1 ») et le cytochrome duodénal b, qui ont été démontrés dans des études précliniques sur les inhibiteurs de PHD1/2 menées par d'autres. Ainsi, l’inhibition de PHD1/2 s’attaque à la fois à une production altérée d’EPO et à une carence fonctionnelle en fer.
L'inhibition de PHD1/2 pourrait réguler positivement l'expression de plusieurs gènes du métabolisme du fer, tels que le transporteur de métaux divalents 1 (« DMT1 ») et le cytochrome duodénal b, qui ont été démontrés dans des études précliniques sur les inhibiteurs de PHD1/2 menées par d'autres. Ainsi, l’inhibition de PHD1/2 s’attaque à la fois à une production altérée d’EPO et à une carence fonctionnelle en fer.
Insilico Medicine PHD — Résumé des inhibiteurs de la maladie rénale chronique – Phase I
Nouvelle structure générée par l'IA
- Structure distinctement différente générée par la plateforme de génération de petites molécules d'IA d'Insilico Medicine, Chemistry42
Efficace dans les thérapies mono et combo
- Puissante inhibition enzymatique PHD
- Puissante induction de HIF-1α
- Puissante activité d'induction de l'EPO
- Dose efficace plus faible dans le modèle de MRC de rat
- Atteindre le niveau cible de HGB via un modèle CKD de rat à induction inférieure de l'EPO
Capacité médicamenteuse prometteuse en tant qu’agent oral
- Bons profils ADME in vitro
- Profils pharmacocinétiques prometteurs pour différentes espèces animales précliniques
- Aucun résultat sur les panels KinomeScan et Cerep
Marge de sécurité favorable
- Profils de sécurité in vitro favorables
Indication
L'anémie de l'IRC est une forme d'anémie normocytaire, normochrome et hyperproliférative.
La pathogenèse de l'anémie est une production altérée d'EPO et une carence fonctionnelle en fer. L'EPO est une cytokine glycoprotéique sécrétée principalement par les reins en réponse à l'hypoxie cellulaire, afin de stimuler la production de globules rouges (érythropoïèse) dans la moelle osseuse.
L'utilisation généralisée d'agents stimulant l'érythropoïétine (ASE) a amélioré la qualité de vie globale et réduit le besoin de transfusions sanguines. L'administration libérale d'ASE était associée à un risque accru d'événements cardiovasculaires, de progression de l'IRC, de thrombose de l'accès vasculaire et de mortalité globale. D'autres problèmes incluent le coût élevé des analogues de l'EPO et la résistance associée ainsi que les effets secondaires.
Alternativement, les inhibiteurs de PHD peuvent être utilisés pour traiter l'anémie en améliorant la sécrétion d'EPO via une régulation positive de HIF-1α.
La pathogenèse de l'anémie est une production altérée d'EPO et une carence fonctionnelle en fer. L'EPO est une cytokine glycoprotéique sécrétée principalement par les reins en réponse à l'hypoxie cellulaire, afin de stimuler la production de globules rouges (érythropoïèse) dans la moelle osseuse.
L'utilisation généralisée d'agents stimulant l'érythropoïétine (ASE) a amélioré la qualité de vie globale et réduit le besoin de transfusions sanguines. L'administration libérale d'ASE était associée à un risque accru d'événements cardiovasculaires, de progression de l'IRC, de thrombose de l'accès vasculaire et de mortalité globale. D'autres problèmes incluent le coût élevé des analogues de l'EPO et la résistance associée ainsi que les effets secondaires.
Alternativement, les inhibiteurs de PHD peuvent être utilisés pour traiter l'anémie en améliorant la sécrétion d'EPO via une régulation positive de HIF-1α.
Statut du projet – Phase I
Statut du projet – Activation de l'IND
Un inhibiteur oral de petite molécule de PHD1/2 pour le traitement potentiel de l'anémie de l'IRC. Les études précliniques montrent qu'ISM4808 est bien toléré et démontre une grande puissance pour sauver l'anémie chez les rats atteints d'IRC. Nous avons déposé notre demande d'IND en Chine en juin 2023 et prévoyons de lancer l'essai clinique de phase I fin 2023.
Découvert en tirant parti de notre plateforme Pharma.AI. En engageant l'application de chimie générative grâce à la conception de médicaments basés sur la structure, de petites molécules ont été générées et priorisées ciblant PHD1/2. Découvert comme candidat préclinique pour le traitement potentiel de l'anémie de l'IRC après plusieurs cycles d'optimisation des propriétés physicochimiques ainsi que des profils d'absorption, de distribution, de métabolisme et d'excrétion (« ADME ») in vitro et in vivo.
Un inhibiteur oral de petite molécule de PHD1/2 pour le traitement potentiel de l'anémie de l'IRC. Les études précliniques montrent qu'ISM4808 est bien toléré et démontre une grande puissance pour sauver l'anémie chez les rats atteints d'IRC. Nous avons déposé notre demande d'IND en Chine en juin 2023 et prévoyons de lancer l'essai clinique de phase I fin 2023.
Découvert en tirant parti de notre plateforme Pharma.AI. En engageant l'application de chimie générative grâce à la conception de médicaments basés sur la structure, de petites molécules ont été générées et priorisées ciblant PHD1/2. Découvert comme candidat préclinique pour le traitement potentiel de l'anémie de l'IRC après plusieurs cycles d'optimisation des propriétés physicochimiques ainsi que des profils d'absorption, de distribution, de métabolisme et d'excrétion (« ADME ») in vitro et in vivo.
